- 上海中申國際貿易有限公司,20年外貿進出口代理服務經驗。
- 服務熱線:139 1787 2118
本文詳細解析了出口醫療器械至印度所需的認證及流程,包括印度醫療器械的監管機構,醫療器械的分類,出口印度醫療器械制造許可證的申請,醫療器械標簽的規定,以及出口印度醫療器械的具體流程步驟。
一、印度醫療器械的監管機構
印度醫療器械的監管由衛生和家庭福利部(MinistryofHealth&FW)下屬的中央藥品標準控制局(CentralDrugStandardsControlOrganization,簡稱CDSCO)負責,該機構內部的重要部門是印度藥品管理總局(TheDrugControllerGeneralofIndia,簡稱DCGI),負責制定全國的醫療器械政策。
二、醫療器械的分類
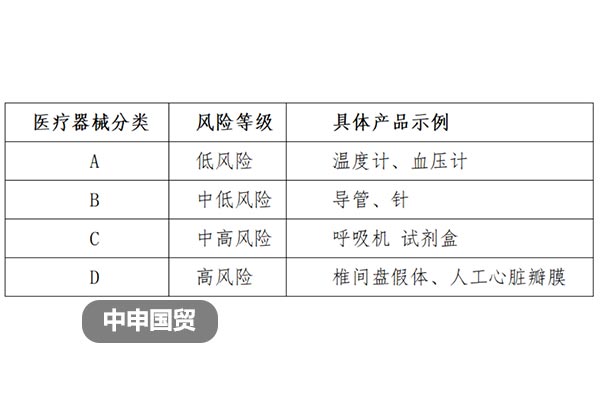
2017年印度公布了《醫療器械管理條例2017》(MedicalDeviceRules2017),參照全球醫療器械法規調和會(TheGlobalHarmonizationTaskForce,簡稱GHTF),將醫療器械分類為A至D四類,對應低至高的風險級別。
三、出口印度醫療器械制造許可證的申請
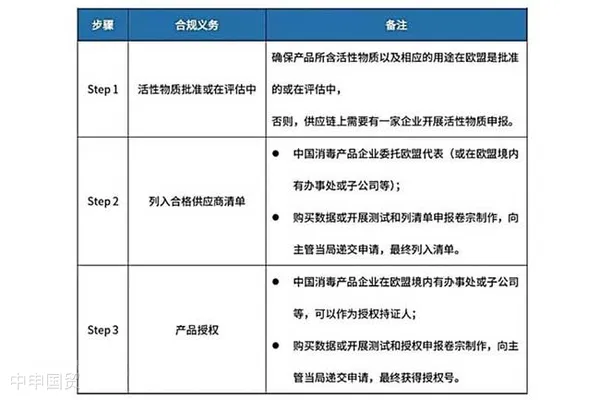
出口至印度的醫療器械必須經過印度當地授權代理人向CDSCO提交醫療器械進口許可證申請。申請流程主要包括以下兩個步驟:
確認生產企業質量管理體系(QualityManagementSystem,簡稱QMS)的符合性:首先,CDSCO會審核授權代理人所提交的生產企業QMS,其必須符合印度醫療器械質量管理標準ICMED13485(修改采用自ISO13485,我國標準YY/T0287等效采用了ISO13485)。該審核包括生產企業QMS技術文件、檢測報告、最近一次現場檢查報告等。如果CDSCO認定生產企業QMS的符合存在疑慮時,可以要求實施評估、產品檢測或生產企業現場檢查(費用由代理人承擔)。
審核醫療器械的安全性與有效性:如果出口印度的醫療器械分類屬于A級或者B級,授權代理人應向CDSCO提交中國的自由銷售證明,或者中國實施臨床測試的數據(或其他可供證明產品安全性與有效性的數據)。如果出口印度的醫療器械分類屬于C級或者D級,授權代理人必須在印度實施臨床測試。例外情況:如果醫療器械(A級至D級)已由歐盟、美國、加拿大、日本或澳大利亞的監管機構頒發了自由銷售證明,則無需再進行臨床測試。
整個許可證申請過程需要細致和精確的工作,包括準備和提交全套文件資料,跟蹤和解答可能出現的問題,以及處理可能的現場檢查和評估等環節。在整個過程中,與CDSCO保持良好的溝通和交流是非常重要的,以確保申請過程的順利進行。同時,對印度的醫療器械法規有深入了解,也是保證申請成功的關鍵因素。
四、醫療器械標簽
印度的《醫療器械管理條例2017》對醫療器械的標簽有著嚴格的規定。其中,第44條到第48條規定了標簽的必備內容:
(1)醫療器械的名稱
(2)用戶識別設備及其使用所必需的細節
(3)制造商的名稱和制造該設備的制造場所的地址
(4)凈數量的準確說明,應以重量、尺寸、體積、單位數量(視情況而定)以及包裝中所含設備的數量以公制表示
(5)生產年月及有效期(或者標簽應標明產品的保質期)
(6)在需要時提供指示,以表明該器械含有藥用或生物物質
(7)提供一個明顯的批號,并以"LotNo.”一詞開頭或"Lot”或"BatchNo.”或"B.No.”
(8)在需要時指出適用于該設備的任何特殊存儲或處理條件
(9)指明該裝置是否以無菌產品形式提供,及其無菌狀態和滅菌方法
(10)給予警告或預防措施(如果認為相關的話),以引起醫療器械使用者的注意
(11)如果該設備是一次性使用的,則應適當標記該設備
(12)如果打算將醫療器械作為免費樣品分發給醫療專業人員,則在該器械的標簽上套印"Physician’sSample—Nottobesold”字樣
(13)除進口設備外,在"ManufacturingLicenceNumber”或"Mfg.Lic.No.”或"M.L”之前加上制造許可證號
(14)如果是進口設備,則在標簽上通過粘貼方式提供(如果尚未打印)此類細節,包括:進口許可證編號、進口商的名稱和地址、實際生產場所的地址以及制造日期
(15)如果小型醫療器械因為體積原因,無法清晰打印所有信息,則至少應包括產品識別和安全所需的信息
五、出口印度醫療器械的流程步驟
出口醫療器械至印度的一般步驟包括:
(1)了解印度的法規要求:研究并理解印度關于醫療器械出口的法規和要求,包括注冊、許可證、標簽要求、質量控制標準等。
(2)注冊和認證:在印度進行注冊和認證,以證明產品符合當地的安全和質量標準。可能需要獲取印度醫療器械管理局(MedicalDevicesAuthorityofIndia)頒發的注冊證書。
(3)準備文件和資料:準備支持出口申請的文件和資料,如產品說明書、質量保證證書、產品測試報告、生產許可證明、注冊證書、產品標簽、企業注冊證明、進出口許可證等。
(4)咨詢和代理:考慮與有印度經驗的咨詢公司或代理合作,他們能提供專業指導,并處理復雜的程序和文件工作。
(5)填寫申請和提交文件:按照印度相關機構的要求,填寫出口申請并提交所需的文件和資料。要確保提供的信息準確無誤,并按時提交申請。
(6)審核和批準:印度相關機構會審核申請和提交的文件,可能會進行檢查、測試和評估,以確認產品符合標準和要求。一旦審核通過,將獲得出口批準。
(7)遵守進口國要求:除了印度的出口要求外,還需了解并遵守目標國的進口要求,這可能涉及到報關、關稅、稅收、進口許可證等方面的事項。
以上步驟可能會因產品類型、國家和法規的變化而不同,因此在出口前,建議尋求專業人士的咨詢,或與當地貿易機構溝通,以確保滿足所有必要的要求。
相關推薦
聯系我們
郵箱:service@sh-zhongshen.com
微信聯系

? 2024. All Rights Reserved. 滬ICP備2023007705號-2  滬公網安備31011502009912號
滬公網安備31011502009912號